Диагностика ВПЧ
Заболевания, вызванные вирусом папилломы человека, относятся к болезням, передающимся преимущественно половым, редко контактным, путем, с латентным началом, хроническим персистирующим течением, и проявляются доброкачественными и злокачественными новообразованиями в зоне входных ворот инфекции. Вирусы папилломы человека - это группа чрезвычайно распространенных и генетически разнородных ДНК-содержащих вирусов, поражающих эпителий кожных покровов и слизистых оболочек.
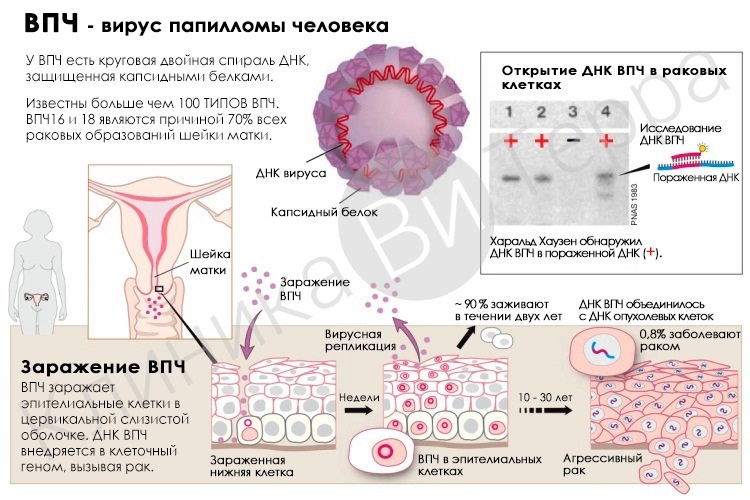
Вирус папилломы человека относится к семейству Рарillоmаviridае. Вирионы не имеют оболочки и содержат двухнитевую ДНК. Геном ВПЧ заключен в белковую оболочку, состоящую из больших (L1) и малых (L2) структурных белков. На основе определения нуклеотидной последовательности генома L1, который кодирует основной капсидный белок, было выявлено и описано более 190 типов ВПЧ.
Каждый тип отличается более чем на 10% от ближайшего родственного штамма. Из их числа более З0 типов ВПЧ могут инфицировать эпителиальный слой урогенитального тракта. В зависимости от онкогенного потенциала выделяют вирусы высокого (типы 16,18, З1,3З, З5,39, 45,51,52,56,58,59) и низкого онкогенного риска (типы 6, 11,42,43,44).
На долю двух высокоонкогенных типов ВПЧ (16 и 18) приходится до 70% случаев РШМ, при этом тип 16 имеет самый высокий канцерогенный потенциал.
“На долю двух высокоонкогенных типов ВПЧ (16 и 18) приходится до 70% случаев РШМ, до 80% рака вульвы и влагалища, до 92% анального рака, до 95% рака ротовой полости, до 89% рака ротоглотки, до 63% рака полового члена”. // Федеральные клинические рекомендации “Вакцинопрофилактика заболеваний, вызванных вирусом папилломы человека”
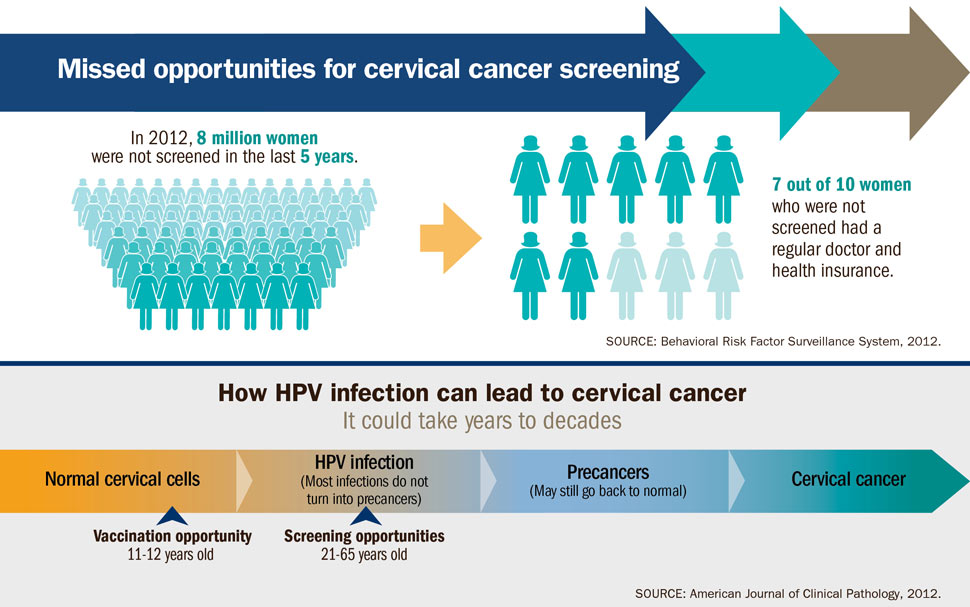
Среди множества типов ВПЧ многие не представляют опасности для здоровья. ВПЧ-инфекции обычно исчезают за несколько месяцев без какого бы то ни было лечения, и примерно в 90% случаев элиминация инфекции из организма достигается в течение 2 лет. В небольшой доле случаев инфекции ВПЧ определенных типов могут принимать хронический характер и со временем приводить к развитию рака шейки матки. Рак шейки матки вне всяких сомнений является самым распространенным из заболеваний, связанных с ВПЧ. Почти все случаи рака шейки матки вызваны ВПЧ-инфекцией1.
80-90% инфицированных ВПЧ высокоонкогенного риска спонтанно элиминируют вирус в среднем в течение 18-36 месяцев без развития CIN. Риск развития предрака и РШМ имеют только женщины с длительной персистенцией ВПЧ ВКР2. С возрастом способность к элиминации вируса снижается, соответственно, повышается риск развития предрака и рака, поэтому рекомендовано регулярное обследование на ВПЧ начиная с 30 лет.
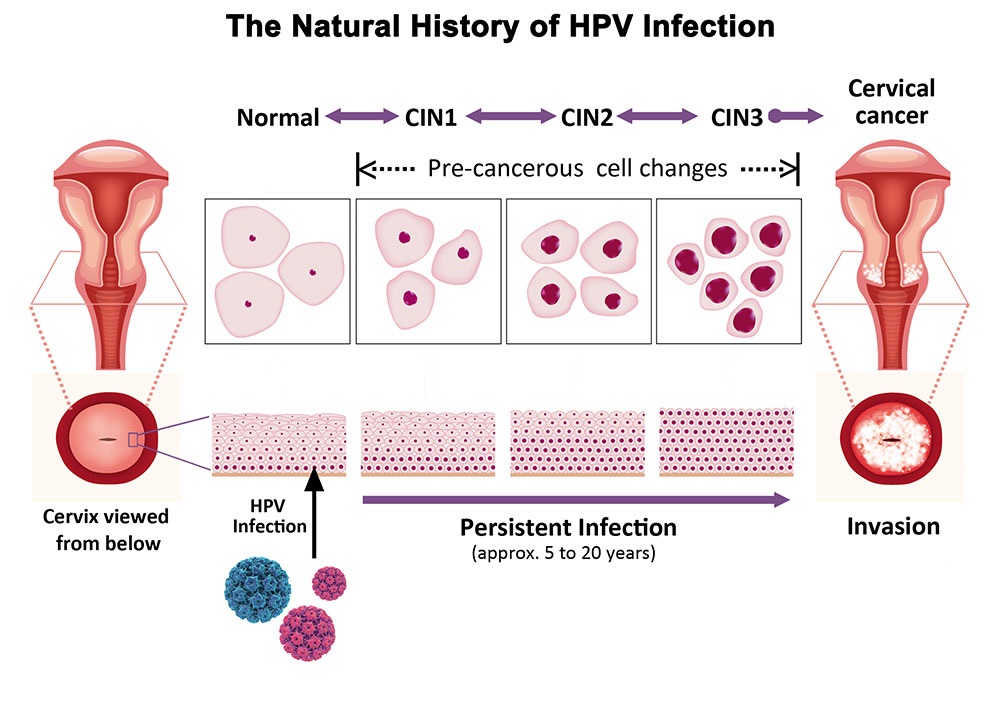
Диагностика скрытой ВПЧ-инфекции осуществляется только методом ПЦР, который позволяет найти ДНК ВПЧ в исследуемом биоматериале. Принцип метода основан на амплификации (многократном увеличении числа копий) специфичного для данного возбудителя участка ДНК. Метод ПЦР с детекцией результатов в режиме реального времени, позволяет определить количество ДНК клинически значимых типов ВПЧ в образце. ПЦР-тест обеспечивает качественное обнаружение вируса папилломы человека в соскобе урогенитального тракта, методом полимеразной цепной реакции с детекцией в режиме «реального времени» с частичным или полным генотипированием.
“Особенностью ВПЧ-инфекции является тот факт, что в силу эпителиотропности вируса он не обнаруживается в крови, а выработка антител иммунной системой отмечается далеко не у всех инфицированных больных. При этом уровень антител очень низок и не способен обеспечить длительный и надежный иммунитет. Это связано со способностью ВПЧ “ускользать” от иммунной системы макрорганизма, что позволяет ему длительно персистировать ввиду своих эволюционно приобретенных особенностей (репликационный цикл ограничен эпителием, нет виремии и цитолиза, локальная иммуносупрессия за счет вирусных белков)”. //Новые возможности ранней диагностики и профилактики ВПЧ-ассоциированных поражений шейки матки. В.Н. Прилепская, Г.Р. Байрамова, Е.А. Коган, Медицинский совет, 2015 г.
Генотипирование ВПЧ дает дополнительные возможности определения прогноза течения заболевания. Необходимость генотипирования может быть оправдана, поскольку выявление нескольких генотипов вируса ассоциировано с менее благоприятным прогнозом течения заболевания и более высоким риском персистенции. Степень онкогенности различных генотипов высокого риска не одинакова. Наибольшей онкогенностью обладают 16 и 18 типы ВПЧ, существуют рекомендации по проведению определения этих двух генотипов вируса после теста на широкий спектр типов с целью более агрессивной тактики ведения пациентов: при выявлении 16 и 18 генотипов рекомендуется сразу проводить кольпоскопическое обследование, при выявлении других типов высокого риска — сначала проводить цитологию, и только при положительном результате цитологии проводить кольпоскопию. Проведение генотипирования позволяет отличить реинфицирование от персистирования инфекции при повторном визите пациента. Получать подобную информацию тем более важно, так как опасность представляет именно хроническая персистентная форма инфекции, недавнее же инфицирование, наиболее вероятно, спонтанно излечивается. О реинфицировании говорит изменение спектра генотипов, о персистирующей инфекции — сохранение генотипа вируса через год после первого тестирования; повторное инфицирование тем же генотипом вируса после самостоятельного излечения практически невозможно.
В июле 2018 г. на мировом рынке было представлено около 250 видов ВПЧ-тестов. Однако эффективность далеко не всех из них могла быть подкреплена клиническими исследованиями, а результаты тестирования большей части не были представлены на страницах какого-либо рецензируемого научного периодического издания. Еще меньшее число тестов удовлетворяли международным консенсусным критериям применения такого рода тестов в первичном скрининге РШМ. При этом стоит отметить, что в 2015 г. насчитывалось всего 5 валидированных тест-систем: RealTime High Risk HPV Test (Abbott), Cobas 4800 HPV test (Roche), Onclarity HPV assay (BD Diagnostics), PapilloCheck HPV-screening Test (Greiner Bio-One), HPV-Risk assay (Self-Screen BV) [26], из которых на российском рынке до сих пор представлены только первые два (Abbott, Roche).
Валидированными для проведения скрининга считают тесты, обладающие аналитической доказательной базой и подкрепленные данными клинического применения на уровне, не хуже, чем у 2 референсных тестов Hybrid Capture 2 (HC2, Qiagen) и GP5+/6+-PCR EIA (Labo Bio-medical Products B.V.). В числе сравниваемых параметров: диагностическая чувствительность и специфичность по отношению к CIN2+, сходимость результатов применения. Тест RealTime High Risk HPV (Abbott) удовлетворяет перечисленным критериям; позволяет одновременно выявлять до 14 генотипов ВПЧ высокого онкогенного риска при их присутствии в клинически значимых концентрациях; способен определять наиболее агрессивные генотипы ВПЧ (16 и 18); имеет внутренний контроль реакции, исключающий получение ложноотрицательного результата в случае недостаточного количества клеток в образце или сбоя при выделении/амплификации ДНК; допускает наличие в образце биоматериала крови, а значит подходит для применения в условиях клинической практики на территории РФ3.
Современный цервикальный скрининг включает ВПЧ-тестирование на разных этапах. Использование ВПЧ-тестирования позволяет выявлять значительно больше предраковых поражений по сравнению только с цитологическим скринингом и увеличить межскрининговый интервал до 5 лет. В связи с этим, несмотря на удорожание первого этапа, скрининг с использованием двух инструментов не оказывается более затратным. В условиях предполагаемой повсеместной вакцинации от инфицирования ВПЧ ВКР первичным звеном скрининга станет ВПЧ-тестирование как наиболее эффективный и экономически целесообразный вариант.
Полезные статьи:
-
Which high-risk HPV assays fulfil criteria for use in primary cervical cancer screening (M. Arbyn, P. J. F. Snijders, C. J. L. M. Meijer, J. Berkhof, K. Cuschieri, B. J. Kocjan and M. Poljak)
-
Скрининг рака шейки матки в XXI веке не пора ли отказаться от цитологической диагностики?
-
American Cancer Society, American Society for Colposcopy and Cervical Pathology, and American Society for Clinical Pathology Screening Guidelines for the Prevention and Early Detection of Cervical Cancer (Debbie Saslow, PhD, Diane Solomon, MD, Herschel W. Lawson, MD, Maureen Killackey, MD, Shalini L. Kulasingam, PhD, Joanna Cain, MD, FACOG, Francisco A. R. Garcia, MD, MPH, Ann T. Moriarty, MD, Alan G. Waxman, MD, MPH, David C. Wilbur, MD, Nicolas Wentzensen, MD, PhD, MS, Levi S. Downs, Jr, MD, Mark Spitzer, MD, Anna-BarbaraMoscicki, MD, Eduardo L. Franco, DrPH, Mark H. Stoler, MD, Mark Schiffman, MD, Philip E. Castle, PhD, MPH, and Evan R. Myers, MD, MPH)
-
Screening for Cervical Cancer USPreventive Services Task ForceRecommendation Statement
-
Новые возможности ранней диагностики и профилактики (Прилепская В.Н., д.м.н., профессор, Байрамова Г.Р., д.м.н., Коган Е.А., д.м.н., профессор, Чернова В.Ф., Окушко А.Н., к.м.н. Научный Центр акушерства, гинекологии и перинатологии им. В.И. Кулакова Минздрава России, Москва)
-
Цервикальный скрининг (Дамирова К.Ф., Бебнева Т.Н. )
-
Clinical Validation of the Abbott RealTime High Risk HPV Assay According to the Guidelines for Human Papillomavirus DNA Test Requirements for Cervical Screening (A. T. Hesselink, C. J. L. M. Meijer, M. Poljak, J. Berkhof, F. J. van Kemenade, M. L. van der Salm, M. Bogaarts, P. J. F. Snijders, D. A. M. Heidemana)
1. По данным ВОЗ
2. Клинические рекомендации (протокол лечения) «Доброкачественные и предраковые заболевания шейки матки с позиции профилактики рака», МЗ РФ №15-4/10/2-7676 от 2.11.2017
3. Damirova K.F., Bebneva T.N. Cervical cancer screening (analitical review). Akusherstvo i ginekologiya: novosti, mneniya, obuchenie [Obstetrics and Gynecology: News, Opinions, Training]. 2019; 7 (3). Supplement: 87–92. doi: 10.24411/2303-9698-2019-13912 (in Russian), 2019г.
